5. Дай каждому,
чего у него нет
Многие болезни возникают при недостатке в организме человека веществ,
которые он либо вообще не умеет синтезировать, либо, по тем или иным причинам,
синтезирует или усваивает извне меньше, чем ему нужно. Классический пример
тому - авитаминозы: цинга, пеллагра, рахит, злокачественное малокровие.
Люди страдают от них при нехватке соответственно аскорбиновой кислоты
(С), тиамина (В1), кальциферола (D) и кобаламина
(В12). Причину этих болезней и радикальный способ их профилактики
и излечения открыли гораздо раньше, чем стало известно, какую функцию помянутые
здесь и другие витамины играют в биологических процессах.
Еще обширнее список страданий и аномалий, вызванных гормональной недостаточностью.
По распространенности среди них, несомненно, первенствует диабет, до 20-х
годов нашего столетия - неизлечимая смертельная болезнь. Диабет, как теперь
знают даже малые дети, развивается, если организму недостает инсулина.
Это белковый гормон, который выделяют бета-клетки островков Лангерганса
в поджелудочной железе. Рост концентрации инсулина в крови служит сигналом
об увеличении содержания в ней глюкозы. Этот сигнал - именно он, а не само
накопление глюкозы - побуждает организм ее усваивать. ОБычно диабет развивается,
когда бета-клетки производят недостаточно инсулина. Однако при некоторых
видах диабета инсулина производится достаточно, но по ряду причин организм
теряет к нему чувствительность: сигнал звучит, но его не слышат...
Компенсация инсулиновой недостаточности при диабете -дело куда более
тонкое, чем профилактика и лечение авитаминозов. Витамины служат простетическими
группами или кофакторами ключевых ферментов, и потому их ничем нельзя заменить.
Их нужно съесть или ввести уколом - иного не дано. А возникающее при диабете
узкое место в метаболической цепи можно расшить различными способами (и
это типично для подобных болезней).
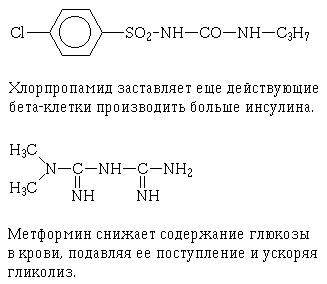
Один из таких способов - заставить бета-клетки производить больше инсулина:
их стимулируют производными фенилсульфонилмочевины. Другой - перекрыть
один из главных источников глюкозы, то есть ее образование из запасного
вещества - гликогена. Этого добиваются с помощью некоторых бигуанидов.
И наконец, третий - компенсировать нехватку инсулина введением его извне.
А для больных, чей организм "глух" к инсулиновому сигналу, приходится
изыскивать иные, обходные способы активировать потребление глюкозы.
Какой вариант лечения уместнее, решать врачу, и только от его умения
и диагностических возможностей зависит, будет ли оптимальный вариант найден.
Сейчас выбор лекарственного препарата и стратегии его применения, как правило,
- более насущная проблема, чем отсутствие подходящих лекарств (оставим
за скобками их высокие цены - фактор, увы, часто влияющий на выбор схемы
лечения).
На примере инсулина, остающегося главным средством против диабета, можно
проследить, как постепенно совершенствуется лекарственный препарат и улучшается
технология его изготовления.
Фармацевтическая промышленность пока не может производить синтетические
белки. Поэтому главным источником инсулина до сих пор служит поджелудочная
железа коров и свиней. Его приходится тщательно очищать, особенно от примесей
других белков, которые могут послужить антигенами и вызвать у диабетика
крупные неприятности с иммунной системой. Кроме того, инсулин животных
хоть и незначительно, но отличается от человеческого, так что иммунные
проблемы даже с идеально чистым бычьим или свиным белком принципиально
неустранимы. Здесь придумано несколько выходов, и все они типичны для современной
технологии лекарств этого типа.
Во-первых, у одной из двух пептидных цепей в молекуле инсулина
свиньи можно удалить концевой фрагмент, в котором сконцентрированы специфически
"свинские" аминокислотные остатки, а потом химическим или ферментативным
путем приделать к этой цепи синтетический "человечий" конец.
Во-вторых, генно-инженерными методами заставляют производить
человеческий инсулин (точнее, белок, который служит его предшественником)
микроорганизмы или даже растения.
Наконец, в-третьих, во многих лабораториях пытаются вычленить
в молекуле инсулина тот фрагмент, который непосредственно вступает во взаимодействие
с инсулиновым рецептором. Если этот фрагмент окажется небольшим, его можно
будет синтезировать в промышленном масштабе.
Наш организм обладает счастливой способностью освобождаться от чужеродных
или ставших ему ненужными веществ. Поэтому принятое лекарство должно успеть
оказать свое действие раньше, чем оно будет выброшено, например, в мочу.
Если же действие лекарства должно быть продолжительным, приходится принимать
его снова и снова либо добиться того, чтобы после однократного введения
лекарства содержание действующего начала в организме достаточно долго поддерживалось
бы на нужном уровне (такие лекарства продленного действия называют пролонгированными).
Гормоны типа инсулина - вроде бы и "свои", и нужны, так что
удалять их как будто незачем. Вспомним, однако, что инсулин - это сигнал.
Регуляция посредством химического сигнала невозможна, если концентрация
его носителя может только возрастать. Поэтому выброшенный бета-клетками
в кровь инсулин все же необходимо непрерывно оттуда удалять, что и делают
разрушающие его протеолитические ферменты (протеазы). Вот почему диабетикам
приходится часто делать инъекции инсулина, что и неприятно, и хлопотно,
а главное, вынуждает их организм существовать в режиме неестественных приливов
и отливов гормона.
Гораздо спокойнее было бы поддерживать концентрацию инсулина в крови
вблизи некоего среднего уровня, а еще лучше - сообразовывать ее с концентрацией
глюкозы. С последней задачей легко справляется современная электроника,
и уже реально существуют устройства величиной с детскую ладошку, которые
состоят из датчика содержания глюкозы, микросхемы, источника тока и дозатора
раствора инсулина. Такое устройство вшивают под кожу, и оно исправно выполняет
обязанности бета-клеток. Правда, цена у него пока такова, что и "новых
русских" насторожит. Вот почему так желательно пролонгировать действие
инсулина и, кстати, многих других лекарств.
Для этого, вообще говоря, придумано множество методов, подчас изощренных.
Например, лекарственное вещество заключают в микропузырьки из бислойной
фосфолипидной мембраны (липосомы) или из полимерных пленок, а то и в микрогранулы
из слабо сшитых полимеров. Из пузырьков и гранул лекарство диффундирует
в кровь, а скоростью этой диффузии можно управлять, изменяя свойства липидной
или полимерной оболочки. Есть и другие "макроскопические" решения,
но мне хочется коснуться хотя бы некоторых чисто химических подходов к
пролонгации.
Один из них - вводить в организм некое неактивное вещество, которое
медленно распадается, высвобождая действующее начало. Это можно уподобить
сбрасыванию маски. Например, упомянутые выше эстрадиол и диэтилстильбэстрол
иногда применяют в виде неактивных ацетатов, которые постепенно гидролизуются
в кровяном русле. Инсулин же для пролонгации его действия вводят в виде
цинковой соли и/или комплекса с протамином - сильно основным белком из
молок рыб.
Другой возможный подход - затормозить выведение лекарства из организма
или его превращение в неактивную форму. С инсулином пока не слишком получается,
однако для некоторых лекарственных пептидов это уже решенная задача. Протеазы
разрезают пептиды точно так же, как и белки, по амидным группам, и часто
самые уязвимые из этих групп можно без ущерба для лекарственного действия
заменить геометрически подобными, но нерасщепляемыми (ну хотя бы -СН2СНОН-).
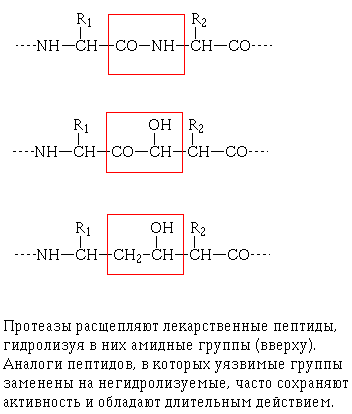
Такая замена возможна потому, что рецепторы часто опознают пептиды не
по присутствию в них амидных групп, а исключительно по бахроме аминокислотных
боковых групп. Эта особенность биологически активных пептидов еще в 60-е
годы привела В.Прелога и Г.Герлаха к удивительно остроумной идее, которую
сейчас используют для получения пролонгированных препаратов. Она заключается
в том, что по расположению боковых групп пептиды близки к своим ретро-энантиомерам,
то есть к таким пептидам, у которых обращена оптическая конфигурация альфа-углеродных
атомов и, одновременно, направление амидных связей в цепи:
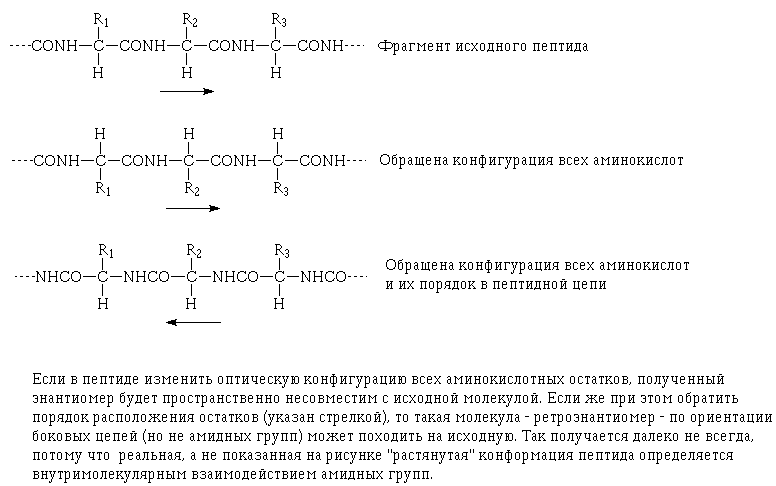
Фокус здесь в том, что протеазы не умеют разрезать пептиды, состоящие
из остатков D-аминокислот, которые в белках не встречаются. Идею Прелога-Герлаха
интенсивно разрабатывали в СССР М.М.Шемякин и Ю.А.Овчинников с сотрудниками.
6. Заказные
убийцы
Пора нам обратиться к самой главной из проблем химиотерапии -созданию
высокоспецифичных лекарственных препаратов, которые воздействуют лишь на
уготованную им мишень, не влияя ни на что иное. Какую область медицины
ни возьми, именно от избирательности биологически активного соединения
зависит в первую очередь его эффективность, а то и сама возможность применения
в качестве лекарства. Именно затем химики изощряются в создании, например,
все новых ганглиоблокаторов, чтобы эти соединения "вырубали"
не все подряд, и даже не "некоторые из..", а вполне определенные
нервные сочленения.
В борьбе за избирательность используются тонкие различия в молекулярной
организации сходных по природе и назначению мишеней, возможности и ограничения
при доставке лекарств к этим мишеням и великое множество других факторов.
Вот пример чисто химического подхода к увеличению избирательности.
Некоторые стероидные гормоны надпочечников влияют на метаболизм глюкозы
(поэтому их называют глюкокортикоидами), но они также обладают противовоспалительной,
иммунодепрессивной и некоторыми другими активностями. Такая разносторонность
талантов сильно осложняет их медицинское применение, ибо оно сопровождается
массой нежелательных эффектов. Особенно много хлопот доставляет вмешательство
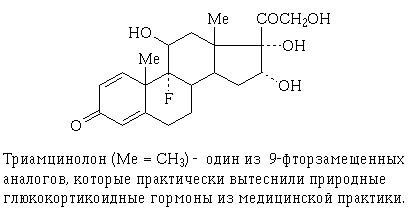
глюкокортикоидов в солевой обмен. Стараниями химиков удалось так модифицировать
их молекулы, что синтетические "мутанты", почему-то гораздо слабее
влияющие на солевой обмен, практически вытеснили из лечебной практики природные
прототипы. Кроме того, получены аналоги глюкокортикоидов, которые плохо
всасываются через кожу. Они удобны для местного применения, ибо позволяют
снимать поверхностные воспаления и аллергические поражения, не наводняя
организм сильнодействующими биорегуляторами. Именно такие аналоги глюкокортикоидов
являются действующими началами хорошо известных мазей "Фторокорт",
"Лоринден", "Синалар".
Наиболее надежный путь к увеличению избирательности открывается по мере
детального изучения механизма действия лекарственного соединения. Именно
так обстоит сейчас дело с нестероидными противовоспалительными препаратами:
индометацином, ибупрофеном, парацетамолом и вечнозеленым аспирином.
Уже давно известно, что эти препараты ингибируют ключевой фермент биосинтеза
простагландина Н2, он так и называется - синтаза. Напомню, что простагландины
и сходные с ними простациклины и тромбоксаны, как и гормоны, служат в организме
короткоживущими носителями химических сигналов.
Совсем недавно выяснилось, что у человека есть две разные синтазы -
деятельность одной из них стимулирует (с помощью простагландина) воспалительные
процессы, а другой - никак с ними не связана.
Разумеется, аспирин и другие аналогичные препараты должны ингибировать
именно первую синтазу, дабы затормозить нарастание воспаления. Они его
действительно ингибируют, но еще сильнее (аспирин - в 150 раз) ингибируют
второй фермент. А он поддерживает нормальное состояние клеток эпителия
желудка и агрегацию тромбоцитов. Вот почему неумеренное применение аспирина
приводит к поражению стенок желудка
Обе синтазы явно различаются специфичностью к ингибиторам; это позволяет
надеяться на то, что окажется успешным поиск более избирательных лекарств.
А за аспирин беспокоиться не надо, ему останется вполне благородное занятие
- профилактика тромбозов. Здесь достаточно очень малых доз, поскольку мишенью
служит синтаза тромбоцитов, в которых ингибированный фермент не возобновляется.
Особого рода избирательность требуется при лечении паразитарных заболеваний,
когда надо истребить возбудителя, не трогая хозяина. В сущности, для исцеления
больного нужно вызвать смертельное заболевание у паразита или хотя бы ослабить
его настолько, чтобы с ним справились защитные системы хозяина. Это возможно
лишь в том случае, если чем-то существенно различаются биохимические процессы,
протекающие в организмах хозяина и паразита. Поначалу даже сам великий
Эрлих сомневался, что этот подход приведет к успеху в борьбе с бактериальными
инфекциями, - уж больно примитивными формами жизни казались ему бактериии
по сравнению даже с трипаносомами и спирохетами. А в примитивных организмах,
по его представлениям, протекают только фундаментальные реакции, общие
для всего живого.
Важный прорыв в этом направлении произошел в 30-е годы, когда в медицинскую
практику были введены сульфаниламидные препараты. История эта весьма драматична
и характерна для мира "рыночных отношений", но это, как говорится,
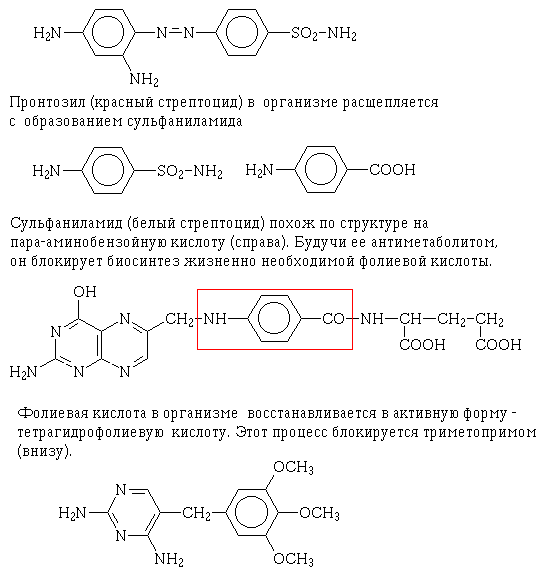
другая песня. А здесь укажем только, что Герхард Домагк в 1935 году неожиданно
сообщил о мощном антибактериальном действии некоего красного красителя
по имени пронтозил. Вскоре стало ясно, что бактерии убивает не сам
пронтозил (памятный старшему поколению как красный стрептоцид; им не только
лечили, но и красили занавески), а продукт его превращения в организме
- амид сульфаниловой кислоты, или, короче, сульфаниламид. Сульфаниламид
широко применяется и поныне, сохраняя в своем названии-противовесе "белый
стрептоцид" память о пронтозиле.
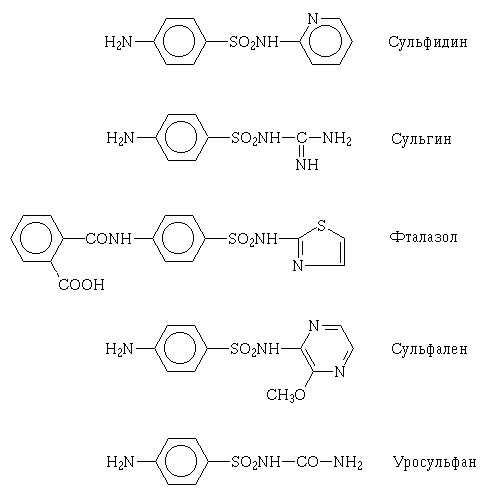
Оказалось, что антибактериальные свойства сульфаниламида сохраняются
при введении заместителей как в амино-, так и в амидную группы. Это развязало
руки химикам, и очень скоро появилось множество сульфаниламидных препаратов,
"настроенных" на определенное применение. Например, сульгин
и фталазол плохо всасываются в пищеварительном тракте и потому особенно
подходят для его дезинфекции. Сульфален очень долго не выводится
из организма и удобен как лекарство с продленным действием. Уросульфан
же, напротив, быстро выбрасывается через почки: его используют против инфекций
в мочевых путях.
В первые же годы применения сульфаниламидов навсегда перестали быть
смертельными такие болезни, как бактериальная пневмония, тяжелые ангины,
дизентерия... Помню, как на пути в эвакуацию моя мать спасла занемогшего
деда, обменяв на станции часики на пакетик сульфидина.
Уже после войны установили, что сульфаниламиды служат конкурентами пара-аминобензойной
кислоты - одного из строительных блоков при биосинтезе фолиевой кислоты.
Такая подмена естественного метаболита его конкурентом - антиметаболитом
приводит к прекращению биосинтеза (метаболическому блоку) фолиевой кислоты.
А она - важнейший кофермент углеродного обмена и абсолютно необходима часто
делящимся микробным клеткам. Поэтому сульфаниламиды останавливают размножение
бактерий - такой эффект называют бактериостатическим.
В последние годы сульфаниламиды часто применяют совместно с триметопримом,
ингибитором другого фермента фолиевого биосинтеза - дигидрофолатредуктазы.
Это позволяет не только уменьшить дозы, но и справиться со штаммами бактерий,
устойчивыми к ингибированию какого-то одного из двух ферментов.
Для человека фолиевая кислота - витамин, иными словами, он ее не производит,
а получает исключительно с пищей. Так что у нас с вами сульфаниламиды никакого
метаболического блока вызвать не могут. Но и бактериям не страшно прекращение
биосинтеза фолиевой кислоты, если они будут получать ее извне. Поэтому
на время лечения сульфаниламидами следует избегать витаминных препаратов,
которые содержат эту кислоту.
Перед сульфаниламидами отступили очень многие бактериальные инфекции.
Многие, но не все... В частности, никак не удавалось подступиться к туберкулезу
и проказе. Однако со временем нашлась управа и на них - тоже с помощью
антиметаболитов пара-аминобензойной кислоты. Вот уже около полувека в арсенал
фтизиатрии входит знаменитая ПАСК - пара-аминосалициловая кислота,
когда-то бывшая единственным средством химиотерапии туберкулеза. Точно
так же уже много лет самым эффективным средством борьбы с проказой служит
4,4'-диаминодифенилсульфон и его производные.
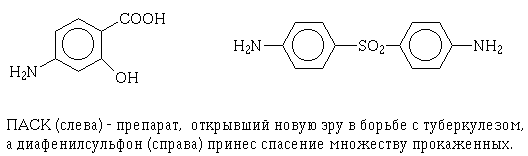
7. Пикник
на обочине
Наконец-то мы с вами добрались до антибиотиков. Так принято называть
производимые микроорганизмами вещества, которые нарушают жизнедеятельность
клеток (иной раз и их собственных!). Вот уже много лет не стихают споры
о биологическом предназначении антибиотиков. Но чем бы ни руководствовалась
эволюция, люди научились использовать антибиотики в своих собственных целях.
Точно так, как в романе Стругацких они пользуются в своих целях странными
и не всегда понятными штуками с места Посещения.
Антибиотиков известны сотни, если не тысячи, но в медицине применяются
лишь немногие, поскольку остальные мало эффективны, токсичны и т.п. По
большей части антибиотики используют при лечении бактериальных инфекций,
и это не случайно, поскольку многие из этих веществ истребляют бактерий,
поражая присущие только им мишени. Парад таких высокоспецифичных лекарств
открывает, разумеется, знаменитый пенициллин, продуцируемый некоторыми
плесневыми грибками.
Жизнь Александра Флеминга и история его великого открытия блестяще описаны
в книге Андре Моруа. Но мы обязаны здесь вспомнить о том, что производство
пенициллина началось во время войны и что этот препарат спас от неминуемой
смерти тысячи и тысячи жертв раневых инфекций. Англичане, честь им и хвала,
не стали таить от союзников существование пенициллина, и советским ученым
во главе с З.В.Ермольевой удалось быстро наладить его изготовление в нашей
стране.
Кстати, о производстве. Выращивать в большом количестве плесневый грибок
и выделять из культуральной жидкости крайне неустойчивый химически пенициллин
не так просто. Казалось, химический синтез будет более технологичен, и
к расшифровке молекулярной структуры пенициллина привлекли лучших химиков.
Отчет этой "оксфордской группы" представлял собой том гигантского
размера, но достигнуть цели чисто химическим путем не удалось. Дело в том,
что, с одной стороны, пенициллин по своему строению не был похож ни на
одно из ранее изученных соединений, а с другой - в ходе обычных химических
манипуляций он с дьявольской изощренностью превращался в другие, не менее
сложные и неожиданные структуры.
Истинное строение пенициллина удалось установить Дороти Ходжкин рентгеноструктурным
методом, а лабораторный синтез осуществили лишь спустя лет пятнадцать с
помощью весьма экзотических приемов и с крайне низким выходом. В результате
пенициллин, как и подавляющее большинство других применяемых в медицине
антибиотиков, производят биотехнологически, выращивая штамм продуцента,
наиболее удобный для культивации и максимально продуктивный по целевому
веществу.
А вот с выяснением причины действия пенициллина исследователи справились
относительно легко, поскольку его результаты бросались в глаза: пенициллин
блокирует у бактерий образование клеточной стенки и они превращаются в
так называемые протопласты. Происходит это потому, что антибиотик препятствует
включению в клеточную стенку одного из ее строительных элементов - дипептида
D-Ala-D-Ala.
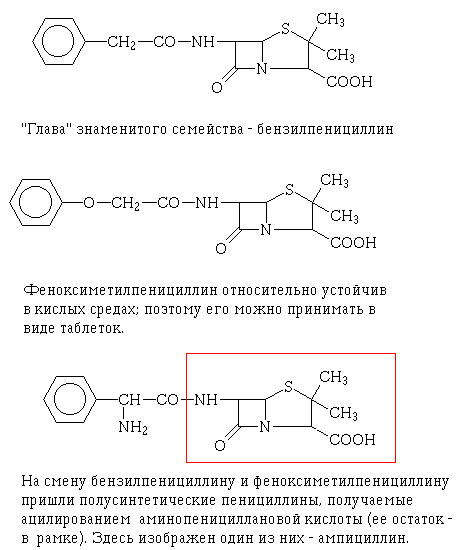
Один из главных недостатков природного пенициллина (он же бензилпенициллин)
- быстрая инактивация в присутствии кислот - объясняется гидролитическим
расщеплением бета-лактамного кольца. Вот почему его не глотали, а вводили
внутримышечно. Позднее удалось остановить биосинтез пенициллина грибками-продуцентами
на стадии аминопенициллановой кислоты и получать из нее химическим путем
разнообразные полусинтетические пенициллины. В них природный остаток фенилуксусной
кислоты заменен на другие ацильные остатки, придающие молекуле те или иные
свойства. Например, одно время был популярен феноксиметилпенициллин,
отличающийся повышенной устойчивостью в кислых средах, - его можно было
употреблять в виде таблеток. Многие полусинтетические пенициллины активны
против болезнетворных микробов, устойчивых к бензилпенициллину.
При эволюционном отборе соединений, которые мы называем антибиотиками,
Природе удалось нащупать одно из главных различий между бактериями и высшими
ороанизмами, прокариотами и эукариотами, - разное устройство их рибосом.
Именно работу прокариотических рибосом, а следовательно, биосинтез белка
в бактериях, избирательно блокируют многие антибиотики самого разного происхождения.
Особенно известны аминогликозидные (стрептомицин, канамицин)
и макролидные (эритромицин, линкомицин) соединения, хлорамфеникол,
тетрациклины. Введение в медицинскую практику этих антибиотиков
в очередной раз открыло новую эпоху в борьбе с инфекциями, поскольку они
обладают значительно более широким спектром действия, чем пенициллин,
Любопытно, что применение антибактериальных препаратов широкого профиля
неожиданно породило некоторым образом обратную задачу. Такие препараты
уничтожают в человеческом организме не только патогенных микробов, но и
всю полезную бактериальную микрофлору пищеварительного тракта, и освободившуюся
экологическую нишу быстро заселяют отнюдь не безвредные одноклеточные грибы.
Вот почему возникла необходимость избирательно подавлять развитие грибов-эукариотов,
не препятствуя в то же время размножению бактерий - естественных спутников
человека. Применяемые для этого противогрибковые антибиотики эксплуатируют
другое различие между эукариотическими и прокариотическими клетками: только
у первых мембраны содержат в качестве обязательного компонента холестерин.
Амфотерицин, нистатин и другие циклополиены этой группы образуют
в мембране комплексы с холестерином, которые представляют собой сквозные
каналы, смертельным для клетки образом нарушающие соотношение трансмембранных
ионных потоков.
К антибиотикам с широким спектром действия метафора "оружие массового
поражения" подходит больше, чем "волшебная пуля". До сих
пор создание препаратов, избирательно подавляющих лишь строго определенных
паразитов, встречает почти непреодолимые трудности. Тем более удивительна
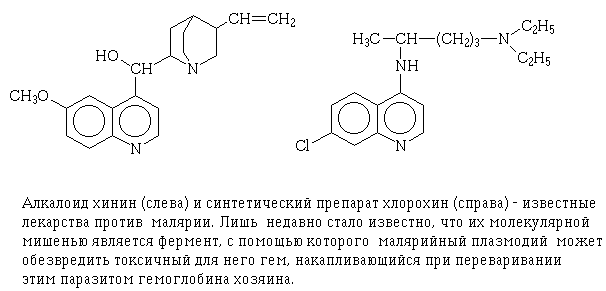
в этом отношении изобретательность Природы. Вот, например, хинин
и его синтетические аналоги вроде популярного хлорохина - едва ли
не единственное средство против малярийного плазмодия, когда он орудует
внутри эритроцитов больного. Главной пищей плазмодию служит гемоглобин,
однако он не умеет расщеплять гем - пигмент, присутствующий в этом белке.
Гем - яд для плазмодия, и тот спасается от отравления, накапливая его в
своей пищеварительной вакуоли, предварительно превратив в нерастворимый
полимер с помощью фермента теломеразы. И только недавно удалось показать,
что хлорохин (как и хинин) специфически ингибиторует теломеразу, оставляя
плазмодий наедине с губительным гемом.
Ингибирование теломеразы требует довольно высокой концентрации хлорохина.
Она достигается благодаря тому, что плазмодий поддерживает в вакуоли низкий
рН, а непротонированные молекулы хлорохина достаточно гидрофобны, чтобы
самостоятельно перебираться через мембраны. Сочетание этих двух факторов
обеспечивает накопление внутри вакуоли протонированной формы хлорохина.
Существуют, однако, мутанты плазмодия, у которых рН содержимого вакуоли
не так низок, и они устойчивы к действию хлорохина.
Здесь мы с вами мы впервые встретились с важнейшим феноменом - появлением
у паразита устойчивости к действию определенного химиотерапевтического
агента. В основе этого явления - высокая частота деления всех одноклеточных
паразитов, а у прокариотов - еще и свойственный только им способ хранения
и передачи друг другу крупных пакетов информации в виде так назывемых плазмид.
Не буду здесь углубляться - для нас важен результат: возникновение и быстрое
распространение устойчивых штаммов вынуждает непрерывно вводить в практику
все новые и новые антибиотики. Более того, на случай, если эпидемию вызовут
штаммы, "привыкшие" к наиболее распространенным антибиотикам,
часть новых и эффективных препаратов приходится придерживать в качестве
боевого резерва.