Голод, взаимное избиение и болезни ограничивают
численный рост человечества и отягчают его существование. Нашей цивилизации
явно не дано излечить социальные недуги, но она, к счастью, одерживает
все новые победы над недугами телесными.
Главным оружием в борьбе с болезнями и в древние
времена, и сегодня служат лекарства. Так принято называть вещества, действие
которых на организм приводит к предотвращению заболевания, исцелению или
хотя бы к облегчению мучений. Поиск эффективных лекарств бесспорно всегда
был и остается одним из самых благородных человеческих занятий, но лишь
в последние годы случайные успехи на этом пути стали уступать место обдуманному
расчету.
Итак, лекарства есть вещества, но и мы, живые
существа, тоже не более чем упорядоченная в пространстве смесь разнообразных
веществ. А одни вещества могут воздействовать на другие единственным способом:
их молекулы должны вступить в химическое и/или физическое взаимодействие.
Поэтому, чтобы лекарство помогло, его молекулы должны встретиться и взаимодействовать
с некими молекулами в нашем организме, которые можно рассматривать как
своего рода мишени.
Обычно мишенями лекарствам служат специфические
компоненты живой материи - как правило, белки и нуклеиновые кислоты. Далеко
не для всех лекарственных соединений известны их мишени, далеко не для
всех пар лекарство-мишень досконально известен характер их взаимодействия,
а о существовании многих мишеней, которые необходимо поразить, пока можно
только догадываться. Вот почему так сложна и драматична история лекарств.
Вспомним, как средневековые алхимики смешивали
наугад вещества и порой наблюдали разнообразные химические реакции. Однако
предсказать ту или иную реакцию и ее продукты можно, только зная строение
и свойства молекул исходных соединений. Точно так же люди случайно находили
и находят в окружающей природе множество целебных начал, но целенаправленно
создавать лекарства возможно лишь тогда, когда есть четкое представление
об их действии на молекулярном уровне. Иначе это всегда будет алхимия,
в какие бы наукообразные формы ее ни облекали.
Самые разные болезни отступают перед лекарствами,
и это само по себе показывает, что покоренные недуги проистекали из-за
неких молекулярных нарушений нормальной жизнедеятельности. В электрических
устройствах все неприятности по большей части возникают от утери необходимых
контактов и появления нежелательных. Можно ли предположить, что в бесконечно
более сложном живом организме у всякого рода разладов, сиречь болезней,
тоже ограниченное число причин? Рискуя быть обвиненным в смертном грехе
упрощения, назову главные из них: отсутствие или недостаток нужных молекул
в нужное время и в нужном месте либо появление или избыток молекул, вредных
в данном месте и в данное время. При кажущейся примитивности такой подход
вполне конструктивен, в чем, надеюсь, вы убедитесь, прочтя эту статью.
1. Вещества
и существа
Живые организмы представляют собой удивительные реакторы, в которых
одновременно протекает гигантское множество разнообразных химических превращений.
И среди этих превращений можно на пальцах одной руки пересчитать такие,
которые протекают сами по себе, без катализаторов. Более того, своего рода
катализаторы требуются организму не только для химических, но и для физических
процессов, например для проникновения ионов и молекул через мембраны или
расплетания спиралей ДНК. Практически все биологические катализаторы -
это белки, их называют ферментами или энзимами. Любое изменение числа молекул
фермента или их каталитической активности сказывается на скорости соответствующего
процесса, а поскольку все процессы в организме взаимосвязаны, - то и на
организме в целом.
Вот хрестоматийный пример. При определенном генетическом дефекте ребенок
рождается с недостаточным количеством фермента, катализирующего одну из
стадий разложения фенилаланина. Если не исключить появление избытка фенилаланина
строгой диетой, продукты его частичного расщепления искажают формирование
мозга и ребенок вырастет идиотом.
Это относительно простая ситуация, в большинстве случаев все куда сложнее.
Дело в том, что в клетках образование и распад самих ферментов и молекул,
регулирующих их активность, в свою очередь контролируются другими ферментами
и эта иерархическая лестница контролеров имеет множество ступеней. На каждой
из этих ступеней возможны врожденные или приобретенные нарушения - отсюда
великое разнообразие заболеваний.
Итак, живой организм - это не столько совокупность белков и других биомолекул,
сколько совокупность обеспечиваемых ими процессов. Останови их - получишь
свежий труп. Измени их скорость - и в зависимости от характера этих изменений
и состояния организма переведешь его в аномальный режим (это и есть болезнь)
или приведешь к норме (сиречь к выздоровлению).
Если общее число молекул ферментов поделить на число ускоряемых ими
реакций, мы получим среднее количество фермента, ответственного за одну
реакцию. Это количество удивительно мало - содержание каждого фермента
в организме обычно не превышает десятитысячных, а то и миллионных долей
грамм-моля. Вспомним, что для катализа вообще характерна ничтожность количества
катализатора по сравнению с исходными веществами (биологи их называют субстратами)
и продуктами реакции.
Лекарства могут вмешаться в жизнедеятельность организма, взаимодействуя
либо с катализаторами-ферментами, либо с субстратами и продуктами определенных
биохимических реакций. Ясно, что большего эффекта при меньших дозах лекарства
можно достичь, целясь именно в катализаторы.
Так обычно и поступают, особенно если субстраты и продукты - низкомолекулярные
соединения. Бывают, конечно, и исключения, но крайне редкие. Скажем, при
желтухе новорожденных в крови резко повышено содержание пигмента билирубина.
И вот для того, чтобы быстро удалить (фактически - сжечь!) билирубин, прямо
в кровь вводят сильнейший окислитель - гипохлорит натрия. Вот еще один
пример - камни в почках обычно состоят из малорастворимых уратов, то есть
солей мочевой кислоты. Они рассасываются при введении в организм (на этот
раз перорально, то есть заглатыванием) ионов лития или органического основания
пиперазина, чьи ураты водорастворимы. Да, чуть не забыл о питьевой соде,
раствором которой иной раз приходится нейтрализовать избыточную соляную
кислоту в желудке.
2. Зачем
траве быть лекарственной?
До начала технологической эры люди успели найти очень много эффективных
лекарств, по большей части растительного происхождения. Наши предки за
тысячелетия отобрали целебные растения и опытным путем определили, когда
их надо собирать и как обрабатывать для получения максимального лечебного
эффекта. Никогда европейцы не сумели бы завоевать и удержать необъятные
колонии в тропическом и субтропическом поясах, не позаимствуй они у южноамериканских
туземцев кору хинного дерева как средство от малярии.
Надо сказать, что на Земле произрастает множество самых разнообразных,
в том числе еще неведомых медицине лекарственных растений, и до сих пор
природа регулярно приносит нам приятные сюрпризы. Так, совсем недавно в
борьбе с раком начали использовать экстракт из тихоокеанского тиса.
Лекарственные растения живут не только в жарких странах, их много и
в наших широтах: это подорожник, ромашка, шалфей, крушина, липа... Некоторые
давно и успешно здесь акклиматизированы, как, например, клещевина, из семян
которой добывают столь любимое и детьми, и взрослыми касторовое масло.
А ведь еще есть и женьшень, и наперстянка, и барвинок - списку нет конца.
Все эти и многие другие лекарственные растения отлично известны народам,
населяющим их ареалы, а со временем сведения о них стали достоянием всего
человечества.
В начале прошлого века усилиями многих ученых было установлено, что
целебное действие лекарственных растений обусловлено присутствием в них
вполне определенных химических соединений, которые стали называть действующими
началами. Так, из коры хинного дерева удалось выделить хинин и цинхонин,
из семян мака - морфин, а из чилибухи - стрихнин.
Именно эти действующие начала стали первыми лекарствами нового поколения.
Их список постоянно расширялся, и вскоре стало возможным сделать важные
обобщения. Оказалось, в частности, что действующие начала можно по их строению
разделить на вполне определенные классы: алкалоиды (обычно довольно сложные
азотсодержащие основания), гликозиды (соединения, в которых разнообразные
по структуре молекулы связаны с остатками сахаров), терпены, стероиды.
Трудно сказать, зачем растениям производить, и подчас в больших количествах,
на первый взгляд совершенно ненужные им вещества. Очень многие из этих
веществ в больших дозах ядовиты, причем не только для человека, но и для
всех теплокровных, а то и для рыб и насекомых. Возможно, с их помощью растения
защищаются от мириад поедающих их существ, от тлей до коров. Слава Богу,
эта защита не всегда эффективна, поскольку именно растения стоят в начале
большинства пищевых цепей, используя при первичном синтезе органических
соединений энергию нашего светила.
О лекарственных растениях известно не только людям, но и животным (в
частности, кошкам), которые при необходимости их разыскивают и потребляют,
сколько должно. Но не все звери столь образованны - домашний скот часто
отравляется алкалоидоносными травами и кустарниками. Известны примеры,
когда действующие начала растений животные используют для самозащиты. Так,
ярко окрашенных бабочек-монархов не склюнет ни одно пернатое - знает, что
они ядовиты. А ядовиты они потому, что еще гусеницами накопили в себе гликозиды
из съеденных листьев, которые в малых дозах нормализуют, а в больших нарушают
сердечную деятельность у теплокровных животных.
Открытие новых лекарственных растений и ранее неизвестных действующих
начал постепенно перестает быть исключительно делом случая или результатом
расшифровки древних рецептов народной медицины. По мере накопления знаний
об особенностях метаболизма растений возрастают предсказательные возможности
химической таксономии - науки, изучающей взаимосвязь между эволюцией растений
и их биосинтетическими возможностями. Культивирование лекарственных растений,
особенно растущих медленно, уступает место производственному выращиванию
культур их клеток, а на смену традиционным методам селекции приходит генно-инженерное
вмешательство.
Есть, однако, и такие проблемы, очертания которых неясны, а путей решения
пока не видно. Конечно, низкий поклон природе, даровавшей нам целебные
вещества, но...
Во-первых, синтетические возможности растений ограничены: при
всей вычурности иных алкалоидов или тритерпенов их структура жестко детерминирована
сравнительно немногими законами биосинтеза (такими, скажем, как ацетатное
правило) и метаболически предопределенным строением отдельных блоков. Если,
создавая эти сложные молекулы, эволюция руководствовалась некими функциональными
критериями (например, отбирались яды для паразитов), то в их структуре
почти наверняка должны быть избыточные элементы, присутствия которых нельзя
было избежать, пользуясь доступным "инструментарием".
Во-вторых, нет уверенности, что созданное эволюцией действующее
начало оптимально как лекарство, если оно отбиралось по смертоносности,
способности кого-то отпугивать или делать что-то еще, пока нам неведомое.
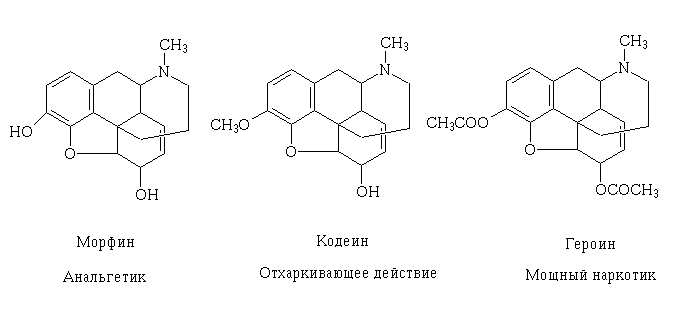
И наконец, в-третьих, хорошо известно, что химическая модификация
действующих начал может кардинально изменить их действие на организм (морфин
- кодеин - героин), однако возможности такой модификации далеко не
безграничны, особенно если учесть необходимые затраты времени и средств.
Все это побуждает задуматься о том, нельзя ли корректировать или планировать
строение действующего начала растения, вмешиваясь в его биосинтез. Быть
может, когда-нибудь, например, станет возможным поручить растительной клетке
или ее химерам самой преобразовывать исходно производимые ею стерины в
глюкокортикоиды (о них - дальше). Сейчас это делают на заводах, комбинируя
химические манипуляции с биологическим окислением промежуточных продуктов
в клетках плесневых грибов.
3. Искать
ключ или сделать отмычку?
Следующий качественный скачок в наших представлениях о лекарствах произошел
во второй половине прошлого века, когда стало лавинообразно нарастать число
и разнообразие синтетических органических соединений. Среди них более или
менее нечаянно удалось обнаружить довольно много эффективных лекарств;
многие из них, например ацетилсалициловая кислота (аспирин), N-ацетил-пара-аминофенол
(парацетамол), пара-ацетаминофенетол (фенацетин), гексаметилентетрамин
(уротропин), 1-фенил-2,3-диметил-4-диметиламинопиразолон (амидопирин),
с успехом используются и поныне. Число таких лекарств постепенно возрастало,
и возникла слабая надежда, что рано или поздно их хватит на все болезни.
На этом этапе никто еще не занимался всерьез совершенствованием найденных
активных соединений - что нашли, на том спасибо...
Успехи иммунных методов борьбы с особенно губительными тогда инфекционными
заболеваниями (чумой, дифтеритом, бешенством и другими) временно затмили
и оттеснили на задний план достижения химиотерапии. Однако она взяла реванш,
когда нашелся ученый, поставивший перед собой совершенно еретическую по
тому времени задачу - сконструировать молекулу соединения, смертельного
для вполне конкретных микроорганизмов - трипаносом.
Пауля Эрлиха вдохновили успехи цитологов, обнаруживших, что разные клетки
и даже разные внутриклеточные органеллы одними красителями окрашиваются,
а другими - нет. И поныне бактерий делят на грам-положительные и грам-отрицательные
в зависимости от того, удается ли их окрасить по методике, которую придумал
датский бактериолог Грам.
Эрлих понял, что биологические структуры различаются по сродству к разным
органическим соединениям, и, следовательно, для каждой из них можно подобрать
вещество, которое она и только она будет связывать. Остается только (только!)
объединить в одной органической молекуле способность к избирательному связыванию
с "ядовитостью", и тогда она, как волшебная пуля, сама разыщет
и поразит мишень. Это была удивительная по своей революционности идея,
поскольку Эрлих и его современники понятия не имели ни о молекулярном устройстве
живой материи, ни о природе ядовитости.
Пауль Эрлих создал такое вещество - убийцу трипаносом, которое заодно
оказалось радикальным лекарством от сифилиса, векового бича грешной части
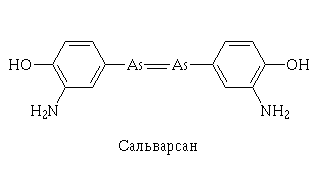
человечества, страшной болезни, вызываемой бледной спирохетой. Это был
3,3'-диамино-4,4'-диоксиарсенобензол - знаменитый препарат 606, впоследствии
получивший заслуженное название "сальварсан" (соединение
латинских корней "спасение" и "мышьяк").
Сальварсан спас множество репутаций и, что гораздо важнее, жизней. Но
история его создания особенно интересна и поучительна, поскольку Эрлих
на много лет вперед определил стратегию и тактику создания новых синтетических
лекарств. Вначале он искал и нашел соединение с нужной, хотя и небольшой
активностью, 4-аминофенилмышьяковую кислоту, но она была весьма токсична
для носителя трипаносом. А потом начался мучительный процесс совершенствования
этой молекулы-прототипа, в ходе которого на ощупь искали пути повышения
активности и уменьшения токсичности. На поиски ушел не один год - недаром
у конечного препарата номер 606.
Кстати, Эрлих потом усовершенствовал сальварсан, и новое лекарство -
неосальварсан - значилось в лабораторном журнале под номером 914.
Впредь подобного каторжного труда не избежит почти никто из создателей
синтетических лекарств.
Оба помянутых выше этапа конструирования лекарственного препарата совершенно
различны по своей природе. Если усовершенствовать прототип - в основном
вопрос терпения и работоспособности, то найти его - во многом дело случая
или озарения. Так обстоит дело даже сейчас, когда, как правило, известны
биомолекулы-мишени, с которыми предстоит взаимодействовать будущему лекарству.
И тем более так было столетие назад - во времена Эрлиха, и даже полвека
спустя - в предвоенные годы, когда о природе и строении этих мишеней не
знали ничего или почти ничего.
4. Слепые
ощупывают слона
Поразительно, что, действуя, по существу, вслепую, химики той поры сумели
угадать очень многое и выработать подходы, разумность которых в полной
мере выявилась гораздо позже. Одним из таких подходов стало упрощение структуры
лекарственных соединений природного происхождения. В самом деле, многие
из этих соединений трудно синтезировать (недаром синтез хинина Робертом
Вудвордом стал вехой в истории органической химии), а растительное сырье
не всегда доступно и дешево. Поэтому было крайне привлекательно вычленить
в молекуле действующего начала минимальный фрагмент, который еще сохранял
бы исходную активность, а заодно установить нужны ли для чего-нибудь остальные
участки молекулы и для чего именно. Вот несколько характерных примеров
плодотворности такой стратегии.
Алкалоид эзерин (он же физостигмин) влияет на работу ацетилхолиновых
синапсов, ингибируя локализованный в них фермент - холинэстеразу. Синтетический
аналог эзерина - прозерин (простигмин) частично воспроизводит
строение эзерина, сходен с ним по своему лечебному действию, а кроме того,
менее токсичен. Его применяют, когда нужно компенсировать ослабленный выброс
ацетилхолина в синаптическую щель или пониженную чувствительность к ацетилхолину
постсинаптической мембраны (например, при миастении).
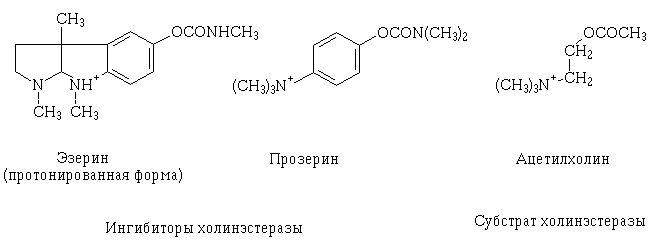
Сравнивая эзерин и прозерин с естественным субстратом холинэстеразы
- ацетилхолином, нетрудно усмотреть сходство во взаимном расположении в
их молекулах четвертичного или третичного аммониевого катиона и группы
-СОО- . Благодаря этому холинэстераза ошибается, принимая эзерин и прозерин
за ацетилхолин. Она связывает их молекулы, да еще так, что их уретановые
остатки оказываются точно на месте, предназначенном для ацетоксильного
остатка ацетилхолина.
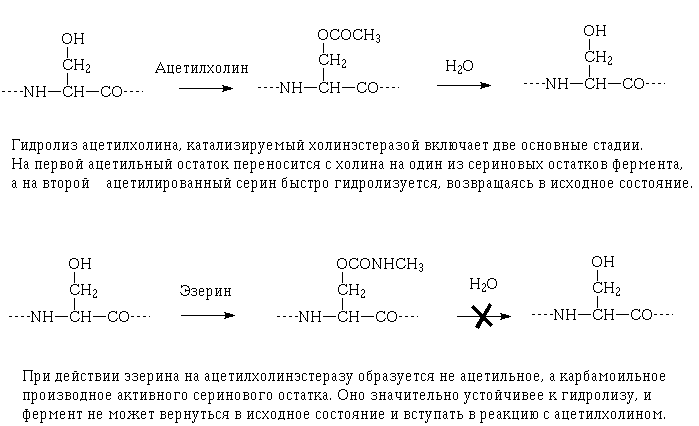
Сейчас мы знаем, что обычно фермент далее переносит ацетильную группу
ацетилхолина на сериновый гидроксил и новый сложный эфир быстро гидролизуется.
Связывание ацетилхолина, перенос ацетильного остатка и гидролиз повторяются
раз за разом, в совокупности составляя нормальный каталитический цикл холинэстеразы.
Обманутый же фермент переносит на гидроксил карбамоильную группу; при этом
образуется уретан, который гораздо устойчивей к гидролизу. В результате
фермент как бы застывает на одной из стадий каталитического цикла, иными
словами, утрачивает свою активность.
Все эти тонкости не были известны создателям прозерина, но вычленить
в молекуле алкалоида ключевые структурные элементы, ответственные за его
активность, они сумели абсолютно точно.
На этом примере хорошо прослеживается сформулированный Эрлихом принцип
волшебной пули: в молекулах обоих ингибиторов холинэстеразы - эзерина и
прозерина - легко выявить "адресующий" участок, который имитирует
ацетилхолин, обеспечивая избирательность связывания с мишенью, и остаток-"убийцу",
который реагирует с мишенью, переводя ее в неактивное состояние.
А вот другая история, тоже связанная с ацетилхолиновым синапсом. Биологическая
функция ацетилхолина состоит в том, что он вызывает открывание катионных
каналов в постсинаптической мембране. В норме эти каналы закрыты своего
рода воротами, которые распахиваются, когда вблизи них связываются молекулы
ацетилхолина. Участки связывания ацетилхолина называют холинорецепторами.
Время жизни комплекса ацетилхолин-рецептор невелико, и после его диссоциации
канал возвращается в исходное закрытое состояние. Управляемые ацетилхолином
каналы - по сути, катализаторы транспорта через мембрану, поскольку одна,
пусть и очень большая, молекула-канал, оставаясь неизменной, пропускает
через себя огромный поток ионов.
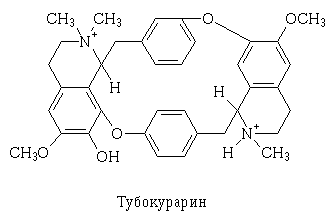
Еще в середине прошлого века Клод Бернар установил, что растительный
яд кураре, употребляемый индейцами для отравленных стрел, нарушает передачу
управлящих сигналов от нервных окончаний к мышцам. Гораздо позднее выяснилось,
что главное действующее начало кураре - алкалоид тубокурарин - успешно
конкурирует с ацетилхолином за связывание с холинорецепторами. Комплекс
рецептора с тубокурарином очень прочен, и, когда доля оставшихся свободными
рецепторов падает ниже некоторого порога, передача сигналов через синапс
блокируется. Структура и расположение холинорецепторов у ворот ионного
канала была неизвестна, однако представлялось вероятным, что в этих рецепторах
есть анионные участки, ответственные за связывание аммониевых групп молекул
ацетилхолина.
Химики предположили, что тубокурарин имитирует сразу две молекулы ацетилхолина,
поскольку в нем две такие группы. Они синтезировали самые разные соединения,
в которых аммонийные группы разнесены точно на такое же расстояние, как
в тубокурарине. Почти все они обладали курареподобным действием. Даже самый
простой из таких аналогов - 1,10-бис-триметиламмоний-декан (декаметоний)
- сохраняет способность прочно связываться с холинорецепторами, хотя в
отличие от тубокурарина не инактивирует канал, а надолго переводит его
в открытое состояние. Правда, при этом передача сигнала через синапс тоже
нарушается, поэтому декаметоний вошел в медицинскую практику как мощный
ганглиоблокатор. Если же в декаметонии укоротить или удлинить углеводородную
цепь между катионными центрами, его активность резко уменьшается.
Было вполне естественно предположить, что оба участка связывания ацетилхолина,
блокируемые тубокурарином и декаметонием, принадлежат к двум разным холинорецепторам,
которые управляют одним и тем же каналом. Это один из самых наглядных примеров
того, как анализ химической структуры лекарственного соединения позволяет
судить о строении биомолекулы, с которой он связывается в организме.
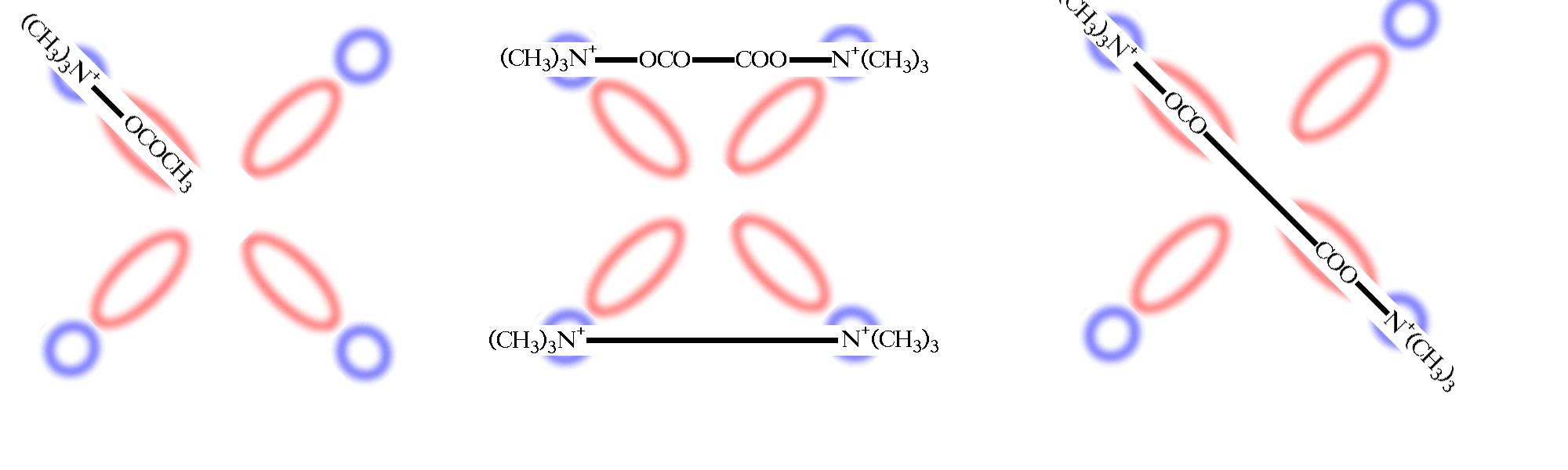
Кстати, эта история имела продолжение. Советский химик М.Я.Михельсон
и его сотрудники обратили внимание на то, что у "двоюродных братьев"
декаметония - бис-эфиров типа (CH3)3N+-CH2CH2-OCO-(CH2)n-COO-CH2CH2-N+(CH3)3
- курареподобная активность имеет два максимума: когда расстояние между
аммонийными группами такое же, как в тубокурарине, и примерно в полтора
раза большее. Они выдвинули смелую гипотезу, что каждый канал обслуживают
не два, а четыре холинорецептора, расположенные крестом, в вершинах которого
находятся анионные центры, а на перекладинах - участки связывания сложноэфирных
остатков. Тубокурарин и декаметоний связываются, попарно соединяя соседние
вершины, а бис-эфир, отвечающий второму максимуму, - противолежащие. Насколько
я знаю, эта гипотеза пока не доказана, но и не опровергнута.
Заметим здесь, что холинэргические синапсы есть у всех животных, но
к "длинному" бис-эфиру чувствительны только синапсы позвоночных.
Возможно, эволюция здесь совершила переход от димерного расположения холинорецепторов
к тетрамерному. Вот как далеко можно зайти, анализируя взаимосвязь между
структурой и активностью лекарственных соединений.
Идея о том, что строение молекулы лекарственного соединения отражает
устройство ее мишени, нашла много подтверждений еще до того, как эти молекулы-мишени
(их принято называть рецепторами) были выделены и изучены. Она объясняет,
почему сходным действием часто обладают вещества, на первый взгляд совсем
не похожие. Причина здесь в том, что в их молекулах есть одинаковые или
похожие по свойствам и размерам группы, сходно расположенные и ориентированные
в пространстве. Именно эти группы и взаимодействуют с общим рецептором.
А остальные элементы структуры - лишние, и их строение не имеет особого
значения: только бы не мешали!
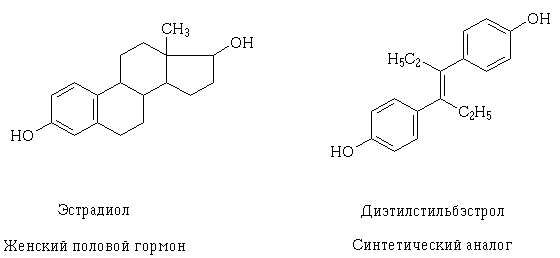
Хрестоматийный пример - транс-изомер диэтилстильбэстрола, который
действует подобно женскому половому гормону эстрадиолу. Их молекулы
очень разнятся, а вот расстояние между двумя оксигруппами и их ориентация
одинаковы.
По мере углубления знаний о структуре белков и других биополимеров,
с развитием энзимологии расширялись и представления о том, как лечить те
или иные болезни, вмешиваясь в биологические процессы, - иными словами,
представления о том, какими могут быть лекарства и их мишени. Биохимия
и фармакология в значительной степени слились воедино: открытие ранее неизвестных
биохимических реакций проясняло природу заболеваний и подсказывало направление
поиска нужных лекарств, а случайные открытия эффективных лекарств побуждали
искать их рецепторы, что приводило к открытию ранее неведомых биологических
процессов и структур.